Adaptation des recommandations GENMAD 2021, ESGE 2019,EHTG/ESCP 2024 et NCCN 2024.
Généralités
- La Polypose Adénomateuse Familiale (PAF) est une affection génétique de transmission autosomique dominante causée par un variant constitutionnel délétère d’un allèle du gène APC (Adenomatous Polyposis Coli). En l’absence de prise en charge adéquate, la PAF est associée à un risque de cancer colique proche de 100%.
- Il existe également des risques augmentés d’autres tumeurs malignes, aux premiers rangs desquelles les tumeurs duodénales, les tumeurs desmoïdes, les cancers de la thyroïde et les cancers gastriques (liés à l’évolution d’adénomes antraux ou de polypes glandulo kystiques (PGK) fundiques.
- La sévérité de la polypose colique peut être variable entre les individus porteurs d’un variant délétère constitutionnelle du gène APC et l’on classe généralement cette atteinte en deux catégories : PAF « classique » (ou FAP dans la littérature) et PAF « atténuée » (ou AFAP). Dans la forme classique de la PAF, les patients présentent une atteinte colique floride faite de plus de 100 adénomes colorectaux synchrones à l’âge de 25 ans. La forme atténuée de PAF est, elle, associée à un nombre d’adénomes moins élevé et à un risque de cancer colique moindre et plus tardif.
- Les patients doivent avoir été vus en consultation d’oncogénétique pour réaliser l’analyse constitutionnelle du gène APC et recevoir les conseils de prise en charge adaptés (modalités de suivi selon l’âge, risque de transmission, possibilités d’accès à un dépistage anténatal). Lorsque la mutation du gène APC est connue dans la famille, le test génétique ciblé est réalisé chez les enfants de personnes atteintes de PAF vers l’âge de 12/14 ans.
- Les patients atteints de PAF doivent être inclus autant que possible dans les réseaux régionaux de suivi financés par l’INCa et en collaboration avec des équipes de la filière maladie rare PolDiGenA (Centre de Référence des Polyposes Digestives Génétiques Adultes).
- Les décisions de prise en charge pour ces patients doivent être discutées en Réunion de Concertation Pluridisciplinaire (RCP).
Prise en charge endoscopique tube digestif bas
Avant chirurgie colique prophylactique
Timing
- La surveillance colique par coloscopie doit commencer entre 12 et 14 ans dans la PAF classique (Option : la surveillance peut être différée à 18-20 ans dans la PAF atténuée (EHTG)).
- En cas de points d’appels cliniques (douleurs abdominales, troubles du transit, hémorragie digestive extériorisée) chez un patient porteur d’un variant APC n’ayant pas encore commencé le dépistage ou chez un apparenté au premier degré non encore testé, une coloscopie doit être réalisée sans délai.
Modalités
- La surveillance doit être réalisée avec un coloscope haute définition en lumière blanche.
- La chromoendoscopie à l’indigo carmin permet une meilleure détection des adénomes et donc une meilleure distinction en PAF classique et PAF atténuée ainsi qu’une meilleure évaluation de la sévérité de l’atteinte rectale.
- Exérèse de tous les polypes de plus de 5 mm.
Rythme
- Annuel.
- Le suivi pourra éventuellement être espacé à 2 ans en cas de forme très atténuée (moins de 20 adénomes, adénomes de très petite taille (1 à 2 mm), patient asymptomatique).
Indications de chirurgie colique dans la PAF
- La chirurgie colique est généralement réalisée à l’âge adulte (20-30 ans) mais peut être parfois avancée en cas d’atteinte profuse ou dégénérée chez des patients plus jeunes.
- En cas de polypose atténuée (AFAP) confirmée sur une coloscopie de bonne qualité avec chromoendoscopie à l’indigo carmin, la chirurgie peut parfois être retardée. Option : Il est possible chez certains patients de poursuivre une prise en charge exclusivement endoscopique (ESGE, NCCN).
- Le choix du type de chirurgie (avec ou sans conservation rectale) dépend de plusieurs paramètres (phénotype rectal et possibilité de résection endoscopique, âge, sexe (fertilité), compliance au suivi, souhait des patients…) et doit faire l’objet d’une discussion en réunion de concertation pluridisciplinaire d’un réseau de suivi régional ou du réseau PolDiGenA après évaluation rectale par une équipe entrainée, de même que la décision de retarder ou de temporiser la chirurgie prophylactique.
Après colectomie avec anastomose iléo-rectale
Timing
La surveillance doit commencer 1 an après la chirurgie.
Modalités
- La surveillance doit être réalisée avec un endoscope haute définition en lumière blanche.
- La chromoendoscopie à l’indigo carmin n’est pas systématiquement recommandée mais permet une
- meilleure détection des adénomes.
- Exérèse de tous les polypes de plus de 5 mm.
- Préparation orale recommandée.
Rythme
- Annuel.
- Le suivi pourra éventuellement être espacé à 2 ans en cas d’atteinte très atténuée du rectum.
Après colo-proctectomie avec anastomose iléo-anale
Timing
La surveillance doit commencer 1 an après la chirurgie.
Modalités
- La surveillance du réservoir doit être réalisée avec un endoscope haute définition en lumière blanche.
- La chromoendoscopie à l’indigo carmin n’est pas systématiquement recommandée mais permet une meilleure détection des adénomes.
- Une attention particulière doit être portée à la zone de transition (possible collerette rectale résiduelle) et aux zones de suture.
- Un examen de l’iléon terminal en amont du réservoir doit être réalisé dans le même temps.
- Exérèse de tous les polypes de plus de 5 mm.
- Préparation orale recommandée.
Rythme
- Annuel.
- Le suivi pourra être rapproché à 6 mois en cas de lésions de dysplasie de haut grade (DHG).
- Le suivi pourra éventuellement être espacé à 2 ans en cas d’atteinte très atténuée du réservoir.
Prise en charge endoscopique tube digestif supérieur (duodénum, papille, estomac).
Timing
- La surveillance du tube digestif supérieur peut débuter à l’âge de 18 ans (EHTG/ESCP) (Option : Réaliser une endoscopie haute lors de la première coloscopie pour évaluation du phénotype digestif haut du fait de rares cas d’atteinte précoce).
- Elle doit débuter au plus tard entre 25 (GENMAD, ESGE) et 30 ans (EHTG/ESCP).
Modalités
- La surveillance du tube digestif supérieur vise à examiner l’ensemble du duodénum (si possible jusqu’à la première anse jéjunale (GENMAD)) la papille et l’estomac.
- Papille :
- Pour la visualisation de la papille il est recommandé d’utiliser un duodénoscope.
- Pas de biopsies systématiques de la papille.
- Ampullectomie formellement recommandée si ampullome > 10mm et/ou DHG et/ou d’évolutivité rapide.
- La surveillance post ampullectomie endoscopique est la même que pour les ampullomes sporadiques : à 3 mois, puis 6 mois, puis 12 mois, puis tous les ans pendant 5 ans.
- Duodénum hors papille :
- Pour un examen complet du duodénum il est possible d’utiliser un coloscope pédiatrique.
- La chromoendoscopie à l’indigo carmin permet une meilleure visualisation des adénomes duodénaux.
- Exérèse de tous les polypes duodénaux de plus de 10mm (GENMAD, ESGE). (Option : Possibilité d’enlever aussi les polypes de 5 à 10 mm (EHTG/ESCP)).
- Estomac :
- Exérèse de tous les adénomes gastriques de plus de 5 mm.
- En cas de polypose glandulo kystiques, être particulièrement attentif en cas de tapis continu de PGK, de polypes de grande taille (>2cm) ou d’amas de polypes coalescents qui sont associés à des risques de dysplasie.
- Pas d’intérêt démontré à l’exérèse systématique des PGK mais discuter en centre expert leur exérèse endoscopique en cas de polypes de grande taille ou de pit pattern différent (EHTG/ESCP).
Rythme
- L’intervalle entre deux examens de surveillance dépend de la sévérité de l’atteinte duodénale et gastrique et de la présence ou non d’un ampullome avec des intervalles de surveillance pouvant aller de 6 mois à 5 ans.
- Pour le duodénum l’intervalle entre deux examens est basé sur le score de Spigelman mais doit être pondéré en cas de présence d’un ampullome (Cf. Figure 1).
- Pour l’estomac, l’intervalle de surveillance est calqué sur le rythme de la surveillance duodénale sauf en cas d’exérèse de lésion(s) significative(s) qui peuvent indiquer un contrôle anticipé :
- Si lésions de dysplasie de bas grade au sein d’un adénome antral ou d’un polype glandulokystique : contrôle anticipé (intervalle variable de 3 à 6 mois (EHTG) à 1 an (NCCN) voire 3 ans en cas de DBG au sein d’un PGK infracentimétrique (NCCN)).
- Si lésions de dysplasie de haut grade au sein d’un adénome antral ou d’un polype glandulokystique : contrôle entre 3 à 6 mois (Option : discussion après évaluation en centre expert de l’indication d’une chirurgie gastrique (EHTG) en cas de PGK avec DHG (NCCN)).
- La prise en charge d’une atteinte gastrique, particulièrement en cas de discussion d’une indication chirurgicale, doit faire l’objet d’une discussion en réunion de concertation pluridisciplinaire d’un réseau de suivi régional et/ou en RCP nationale du réseau PolDiGenA.
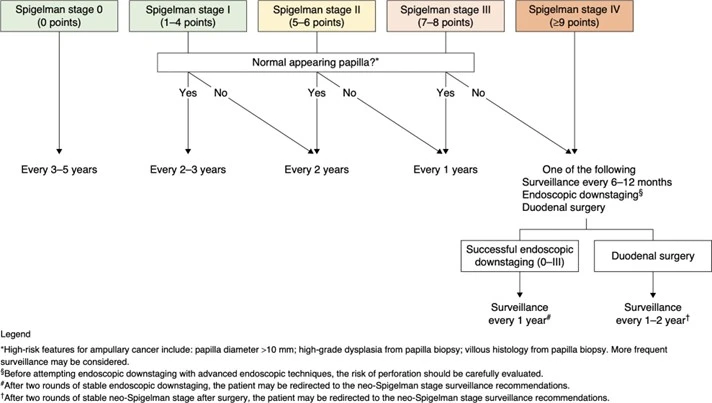
(Tiré des recommandations EHTG/ ESCP 2024, ® Zaffaroni et al, BJS 2024, avec l’aimable autorisation des auteurs)
NB : Ces recommandations sont relatives à la surveillance systématique mais tout point d’appel (anémie, rectorragies ou méléna, douleur abdominale, amaigrissement inexpliqué…) doivent amener à rapprocher les examens lorsque cela est indiqué.
Recommandations générales d’arrêt du tabac, de lutte contre la sédentarité, d’activité physique régulière, de
correction de la surcharge pondérale.
Références
- van Leerdam Monique E. et al. Endoscopic management of polyposis syndromes : European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy 2019;51:877-95.
- Zaffaroni Gloria et al. Updated European guidelines for clinical management of familial adenomatous polyposis (FAP), MUTYH-associated polyposis (MAP), gastric adenocarcinoma, proximal polyposis of the stomach (GAPPS) and other rare adenomatous polyposis syndromes: a joint EHTG-ESCP revision. British Journal of Surgery 2024 May 3;111
- Buecher Bruno, Saurin Jean-Christophe, Conseils de prise en charge de la maladie de la polypose familiale liée au gène APC. FICHE GENMAD – 2021
- Gupta S. et al. NCCN Guidelines Version 3.2024 Genetic/Familial High-Risk Assessment: Colorectal, Endometrial, and Gastric
- Friederich P, et al. Risk of developing adenomas and carcinomas in the ileal pouch in patients with familial adenomatous polyposis. Clin Gastroenterol Hepatol. 2008 Nov;6(11):1237-42.
En collaboration avec le réseau PolDiGenA.
Auteur : Marion DHOOGE
Relecteurs : Bruno BUECHER, Bertrand BRIEAU, Estelle CAUCHIN, Frédérick MORYOUSSEF, Jean-Christophe SAURIN
Juin 2025